
19世纪著名医生William Osler已经说过:“好的医生医治疾病,而伟大的医生医治得病的患者。”但在20世纪,医学界通常将患者视为一系列症状的集合,而不是一个集体。这种状况随着医疗效劳零碎的开展而加剧,它让患者的护理变得零散
数字安康有能够使William Osler医生以患者为中心的护理愿景变为理想。数字安康工具有宏大的潜力,可以进步我们精确诊断和医治疾病的才能,并增强对团体的医疗效劳,真正做到以患者为中心。
我们经常倾向于高估一项技术的短期影响,却低估它的临时效应。 在我看来,数字安康的将来就是如今。 FDA正在采取一些新的措施,以确保能从中受害。最值得留意的是, 我们正在扩展数字医疗工具的时机,使之成为药物审查的一局部, 并将这些才能与药物递送结合,构成药物递送零碎。
我们正在经过新的事后认证项目,来扩展作为医疗设备的数字安康工具的上市前审查新形式。我们正在施行一种新的办法,来审查人工智能。我们还宣布了一项新的数字安康工具,来使用于我们本人的任务——药物平安性的上市前审查。最初,我们正在推出一个新的数字安康孵化器。我会顺次谈谈这些举措,以及它们如何树立在我们更宽广的视野之上。
弱小的数字安康技术曾经失掉推行,其它技术也会在将来几年失掉推行。例如,挪动安康使用顺序(apps)曾经在协助消费者管理本人的安康,经过更好地控制饮食和生活方式。越来越多的挪动安康apps在糖尿病预防、哮喘和成瘾恢复等范畴显示出前景。依据业内估量,到往年年底,美国50%的智能手机战争板电脑用户会下载挪动安康apps。
除了给患者赋能,数字工具也经过新的数据流为医生提供理解患者安康情况的片面视角。这些工具正在改动医生的任务流程,为患者提供更好的护理。 2017年,FDA共同意了51款数字安康产品, 这反映了连通和顺畅监测的趋向。这些产品中包括一款可以嵌入肉体分裂症药物的传感器,这让患者可以经过医疗apps与医生共享医治数据。
数字安康也能真正改善医疗效果,进步疗效,降低本钱。以支持临床决策的医疗影像软件为例,诊断中风需求分秒必争,由于血栓能够招致患者的功用严重丧失,并添加患者中风的几率。往年2月,FDA同意了一款临床决策支持软件,该软件运用人工智能算法以更快的速度告诉神经血管专家,从而延长诊断工夫,及早采取无效的医治援救患者。
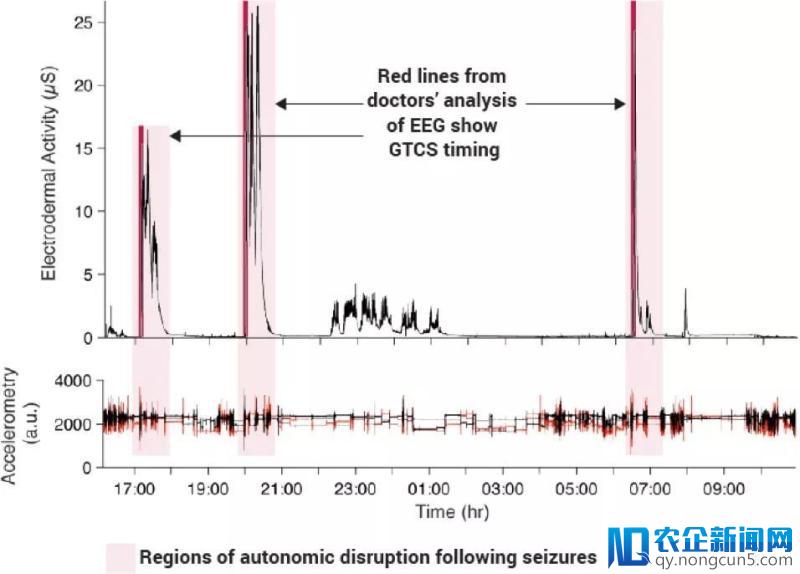
(获批的软件采用人工智能算法,可以剖析出癫痫发作的工夫,图片来源:Empatica)
FDA在支持这种继续创新方面发扬了关键作用,这是我们维护和促进公共安康的使命的一局部。 首先,我们必需确保我们的监管办法能维持我们检验产品平安性的迷信黄金规范。 我们必需一直把维护患者放在任务的首位。
作为使命的一局部,我们还必需采取措施,确保有利的新技术可以被无效推进,并及时为患者提供效劳。由于最终,患者要从迷信中受害。
这意味着我们还必需看法到,FDA的监管办法并不总是合适数字医疗等新兴技术或这一范畴的疾速变化。假如我们希望患者从创新中受害, FDA自身必需像我们正在监管的技术一样具有灵敏性和创新性。
这要求我们在数字安康等高度创新范畴要采取古代灵敏的监管办法,鼓舞更多的研发者将先进技术转化为临床工具,使患者受害。为了协助推进这些时机,我在去年夏天宣布了数字安康创新举动方案(Digital Health Innovation Action Plan)。这一新方案概述了我们为重新设计FDA的办法所做的努力,以确保一切人都能及时取得高质量、平安和无效的数字安康产品。
我努力于将数字医疗作为一种工具来为消费者赋能,并打破制约提供医疗效劳的妨碍。为了扩展这一停顿,我制定了几个关键目的。其中包括添加FDA数字医疗人员的数量和专业知识,在CDRH内推出数字安康软件事后验证试点项目,并发布新指南以完成我们的政策古代化,概述我们推进数字安康创新的努力。
数字安康创新举动方案
我很快乐地宣布,我们曾经在这些目的上获得了本质性的停顿。除了我们所获得的成就之外,我还想宣布几项初次推出的新举措。
我们发布了一项新政策,将简化包括多种功用的数字安康产品的途径, 其中一些作为医疗器械遭到FDA的监管。这项新指南是我们举动方案的另一局部。它解释了FDA对这些多功用数字设备的监管办法和政策,并说明了FDA将会或不会审查这些设备中包括的某些软件,只需它们不会给FDA审查下的功用带来风险或不利影响。
例如,关于检测心脏节律等重要信息并将其传输到患者的电子安康记载的医院监视器,FDA只会审查心脏监护功用,除非传输功用对监护功用的平安性或无效性发生不利影响。在这种状况下,研发者只需求证明他们曾经处理了两种不同功用之间存在的任何潜在不利影响。
我们的目的是让研发者可以无效地将最新技术归入其产品中,同时将FDA的审查重点放在用于诊断或医治的高风险医疗设备的平安性和无效性上。 我们置信这种办法将鼓舞在这个重要范畴获得更多创新。
我很快乐宣布该方案的另一个重要更新。我们曾经获得了任务形式的初稿,它为该方案的各个方面提供了愿景,以及扩展方案的步骤。这一形式曾经在我们的网站发布。我们还分享了一个新的道路图,概述我们将如何开发该方案。
这是我们对这个新方案的任务形式的几次迭代的第一个初级草案。 我们需求推进的关键局部是来自研发者、患者、医生和大众的意见。 因而,在整个任务形式中,你会看到我们曾经制定了关于该方案各个局部需求答案和意见的“质疑成绩”。我们设计的Pre-Cert项目是一个迭代的协作式体验,你的反应是其成功的关键。
我们努力于在2018年底推出“Pre Cert 1.0”,这是该方案的首个版本。一旦我们牢牢掌握了这个框架,会在2019年对其进一步完善。
启动将数字安康使用于药物的方案
我宣布我们将扩展时机,运用数字安康工具作为药物开发的一局部,并在这个进程中完成新的创新,以改善患者的护理。
当我们初次开端讨论数字安康在药物开发中的作用时,我们将努力确保我们的监管办法能反映这些产品的新颖性,并鼓舞和支持他们的创新。 我们必需看法到,数字安康有潜力成为进步药物递送平安性和无效性的新工具。
我们晓得,为了完成这些机遇,我们需求制定明白的政策,以确定如何将数字安康工具的审查和验证归入药物开发方案。
与特定药物相关的挪动设备和软件可以协助患者继续承受医治,由于药物依从性历来是一项应战。 例如,它可以协助患者和医生确认患者曾经服用了药物,并且可以很容易地将信息整合到电子安康记载中。再举一个例子,软件可以协助癌症患者监测医治的反作用,经过运用智能手机摄像头和面部辨认软件来客观分类疼痛症状,并追踪认知表现。

(可以追踪肉体分裂症患者服药状况的Abilify MyCite零碎,图片来源:Proteus Digital Health)
它也可以让开发者恪守上市后的监视要求。在某些状况下,这些工具可以经过嵌入智能设备中的软件或传感器搜集数据,以支持平安性和无效性声明。
为了协助扩展数字安康的潜力来完成这些能够性,我们将经过新的指南来推进这方面的政策框架。我们将向大众咨询意见,如何将软件使用于处方药中,FDA如何促进数字安康功用开展的创新,以及如何将这些创新产品整合到患者的初级医治选择中。我们还将咨询意见,如何支持那些作为同意药物一局部的数字安康工具的开发,以及如何在软件阅历疾速更新的进程中妥善停止监管。
FDA将开放一个公共档案,以寻求开发这些前沿技术的创新者互联网电子商务和移动商务消费渠道的普及,使得支付市场将在不久的将来继续呈现更加美好的增长前景。的意见,以及希望从这些提高中受害的医生和患者的意见。
我们在FDA的使命是在一个均衡、基于风险的框架下,使用我们的规则,既能维护患者,又能使处方药中的数字化蓬勃开展。
最终,我们树立此框架的目的将是开发审查和同意数字安康工具的无效途径,作为药物审查的一局部,以便这些工具充沛发扬潜力协助我们医治疾病,并鼓舞软件和医治的协作。
人工智能
人工智能(AI)是数字安康时代最具潜力的工具之一,特别是机器学习(machine learning)。FDA正在积极开发新的监管框架,以促进这一范畴的创新,并支持运用基于人工智能的技术。因而, 当FDA使用Pre-Cert方案时,将思索到机器学习的最大优点之一:持续学习和改良的才能 。对AI采用Pre-Cert方案,可以允许公司对其设备停止一些小的更改,而不用每次都提交审核请求。而且,FDA将确保监管框架的其它方面(如新的软件验证工具)具有足够的灵敏性,以跟上这个迅速开展范畴的共同属性。FDA对AI的监管是为了给患者树立适当的维护,确保这些新技术可以到达其平安性和无效性规范,从而为患者带来好处。假如它不具有维护和改善患者状况的才能,这项技术就不会被FDA认可。
FDA估计, 将来几年将会有越来越多的基于AI的工具提交审核请求,首当其冲的是医疗成像设备。 FDA对AI的态度也将着重关注其处置理想世界数据的办法,包括来自病理幻灯片、电子病历、可穿戴设备和保险索赔数据的构造化和非构造化数据。FDA以为,随着更多的真实世界数据被输出到AI算法中,AI工具可以变得更具预测性。
AI也有能够明显降低由慢性疾病并发症引发的本钱。 比方说,糖尿病视网膜病变是招致3000多万糖尿病患者视力丧失的最罕见缘由,也是任务年龄段的成年人视力妨碍和失明的次要缘由。停止晚期筛查是预防严注重力成绩的关键,但大约一半的糖尿病患者都未遭到眼科医生的反省。最近,FDA同意了第一款将特殊照相机和AI相结合的医疗设备,用于检测糖尿病成年患者的轻度糖尿病视网膜病变。假如AI检测到细微视网膜病变,患者的主治医生就可以将他们转诊给眼科专家停止进一步的反省医治,以防开展出严重结果。
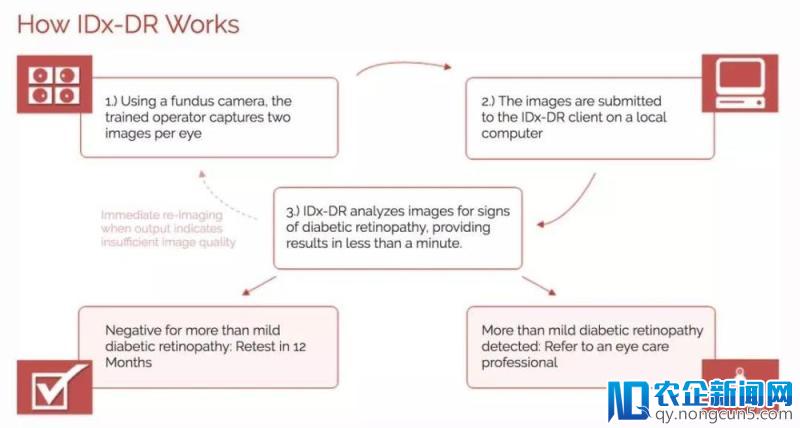
(往年4月,美国FDA同意了首款运用人工智能检测糖尿病患者视网膜病变的医疗设备IDx-DR,图片来源:IDx官方网站)
将来,AI工具可以直接集成到智能手机或可穿戴设备中用于各种晚期检测使用,从而增加昂贵的专科门诊费用,同时添加尽早发现潜在严重成绩的能够性。为了跟上这些疾速开展范畴的创新步伐,FDA自身必需在外部应用数字医疗工具来开发新的监管工具。这些数字工具可以协助FDA使药物和设备的开发愈加高效、可预测,并且更能反映患者的真实世界体验,同时简化F我国这片创新热土正在发生一场全面而深刻的产业结构变革。DA的任务流程,并将协作变得愈加容易。
推出新的上市前数字平安方案
FDA这次推出了一项新的上市前数字平安方案(Premarket Digital Safety Program)。该方案针对新药研讨请求(IND),要求其根据减速平安报告规则,到达IND电子报告的数据规范。这个方案首先在FDA的肿瘤杰出中心(oncology Center of Excellence)以及该机构的药物和生物制剂中心测试。
采取这个方案是由于传统的审核方式亟待改动。在传统审核中,IND的临床实验主办者必需在15天或7天外向FDA和参与调查的人报告严重和不测的疑似不良反响,详细取决于事情类型和严重水平。FDA在IND阶段的次要义务之一是确保患者平安。但模糊不清的流程招致任务效率低下。实验主办者向FDA提交PDF或许纸质版的上市前平安报告,审查员必需辨别审阅每个报告,阅读数以千计的记载,来理解受试新药的平安性。审查员破费一大块工夫来管理这些平安报告,而不是检测信号和审查医疗后果。这个进程不契合数字时代的要求。
因而,FDA最近展开了一个成功的试点,开发并证明了采用数字提交的可行性,在该进程中,将上市前平安报告作为易于可视化和剖析的数据集传输给FDA。FDA置信,新的数字框架可以明显进步上市前平安审核流程的效率和精确性,当该方案片面施行时,每个月可节省数百小时的审核工夫。
推出新的FDA数字安康孵化器
最初,为了将数据剖析整合到监管决策中,FDA正在迈出新的一步,即创立一个名为INFORMED的外部数据迷信孵化器(Information Exchange and Data Transformation)。这个新科技孵化器最后的重点,是在安康技术和癌症相关的范畴停止监管迷信研讨,目的是推进数字安康工具的框架。正在停止的INFORMED项目是与Project Data Sphere协作的,后者是一个非营利性的开放式癌症数据库,目的是应用医学成像数据开发肿瘤动力学分类算法。FDA还与美国国度癌症研讨所(NCI)协作展开结合研讨,设计和开发数字生物标志物作为药物开发工具,这些根底研讨类型将引导行业向前开展。另外,FDA还与哈佛在AI和机器学习范畴展开了一项研讨项目,重点是设计、开发和施行针对监管迷信使用的机器学习和AI算法。
FDA采取的这些改良将推进创新开展。我们都晓得,创新的最大妨碍是新产品开发的本钱和风险。将有前景的想法转化为产品,以延伸和改恶人类生活,能够需求数十年的工夫。而新的数字工具可以协助降低本钱和风险,将产品与最能够受害的患者停止婚配,或更快地辨认潜在的严重反作用。新的数字工具可以打破研讨和理想世界之间的人为妨碍,对两者都发生裨益。因而,这些技术也促使FDA重新考虑本人的使命,以及如何在这个新颖的范畴完成平安无效的创新。
本周精彩引荐
银川互联网医院“有人管”了,复盘2014年至今树立的55家互联网医院
原始激动之后,也该让诊所“垄断”一下了
杠杆在上,支点在下,看第三方独立医疗机构玩家如何四两拨千斤
亿欧引荐:2018年6月13-15日,由上海市经济和信息化委员会、上海市商务委员会、上海市长宁区人民政府指点,上海市长宁区青年结合会和亿欧公司结合主办的“ 2018全球智能+新商业峰会 ”将在上海长宁世贸展馆举行,诚邀各位一同助力“AI落地,产业晋级”。
活动概况: 2018全球智能+新商业峰会

